AI 신약 개발 로드맵은 일반적으로 3년간의 성장 전략을 포함하며, 1년차에는 PMF 탐색 및 파일럿, 2년차에는 임상 및 규제 준비, 3년차에는 허가와 글로벌 시장 진출을 목표로 합니다. 실제 정책 및 시장 동향을 반영한 구체적인 실행 계획이 중요합니다.
AI 신약 개발, 1년차 PMF 탐색 및 파일럿은 어떻게 진행되나요?
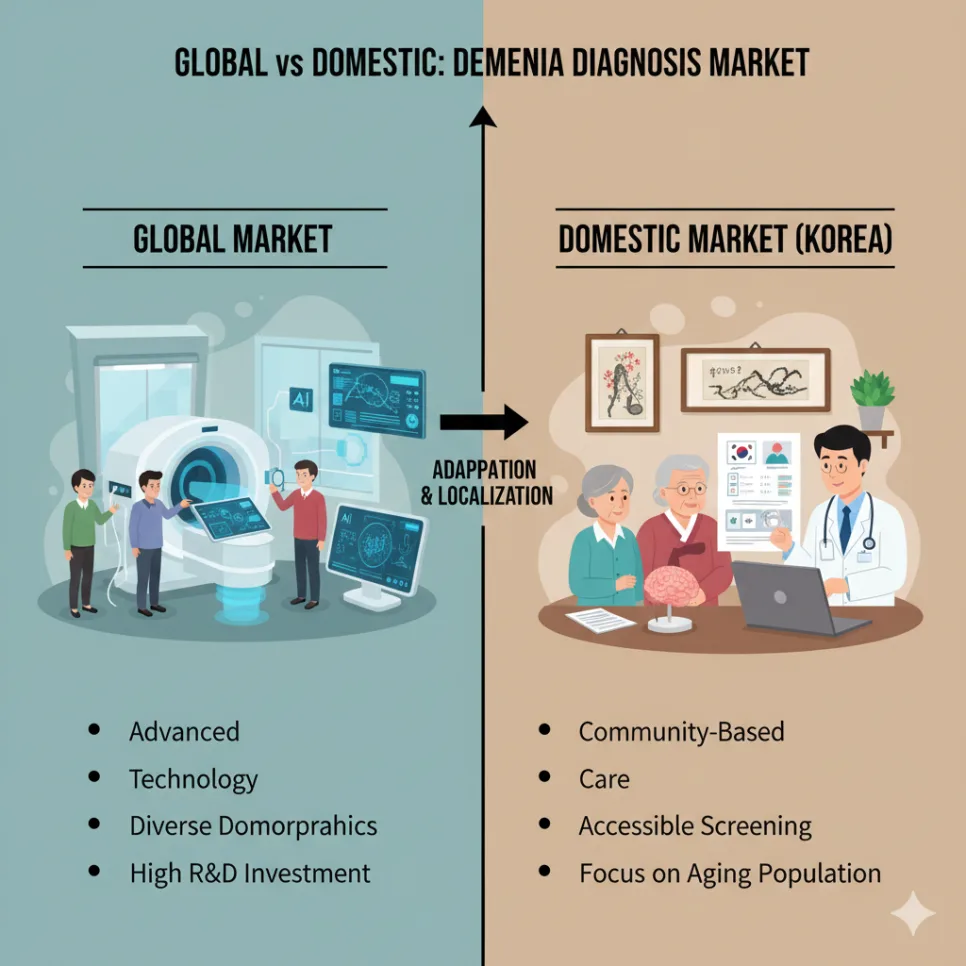
1년차에는 AI Hub 데이터와 공개 코호트 데이터를 활용하여 프로토타입 모델을 개발하는 데 집중합니다. 예를 들어, 치매 진단 의료 영상이나 인지 기능 음성 데이터를 기반으로 초기 모델을 구축할 수 있습니다. 이후 1~2개 지자체 또는 관련 기관과 협력하여 파일럿 또는 시범 사업을 진행하며, 알츠윈의 경기도 및 전주시 사례처럼 '고위험군 발굴'과 같은 구체적인 성과 지표를 만드는 것이 중요합니다. 이 과정을 통해 시장 적합성(PMF, Product-Market Fit)을 탐색하고 초기 데이터를 확보합니다.

AI 신약 개발, 2년차 임상·규제 준비 및 레퍼런스 확대는 어떻게 해야 할까요?
관련 글
2년차에는 실제 임상 데이터(RWD, Real-World Data)를 기반으로 모델의 민감도, 특이도, AUC 등의 성능 지표를 논문화하는 데 주력합니다. 또한, 식약처의 디지털의료기기 가이드라인 및 디지털 치료제(DTx) 관련 보고서를 면밀히 검토하여, 개발 중인 AI 솔루션이 의료기기로서의 가능성이 있는지, 혹은 디지털 치료제로서의 가능성을 더 높일지 전략적인 방향을 결정해야 합니다. 디지털 치료제 기술 동향 보고서에서 강조하듯, 임상적 유효성 입증과 규제 당국의 요구사항 충족을 동시에 준비해야만 제약사, 보험사 등과의 협력을 성공적으로 이끌어낼 수 있습니다.

AI 신약 개발, 3년차 허가·글로벌 진출 및 수가 논의는 어떻게 준비해야 하나요?
3년차에는 국내 허가 획득과 더불어 해외 시장 진출을 위한 전략 수립이 필요합니다. 세븐포인트원이 알츠윈을 FDA에 등록하여 글로벌 신뢰도를 확보한 사례처럼, 미국, 일본 등 주요 해외 시장의 인증을 염두에 둔 접근이 중요합니다. 한국건강증진개발원 및 제약바이오협회 보고서에서 제시하는 것처럼, 아직 수가 체계가 명확히 확립되지 않은 상황에서는 정부 기관(B2G) 또는 기업 간(B2B) 사업을 중심으로 성장을 도모하는 것이 현실적입니다. 향후 수가 논의가 본격화될 경우, 급성장할 수 있는 기반을 미리 마련하는 것이 중요합니다.
AI 신약 개발 로드맵 실행 시 주의할 점은 무엇인가요?
AI 신약 개발 로드맵을 실행할 때는 기술 개발뿐만 아니라 규제 환경 변화와 시장의 수용성을 지속적으로 파악하는 것이 중요합니다. 특히, 임상 데이터의 질과 양은 모델의 신뢰도 및 허가 과정에 직접적인 영향을 미치므로, 데이터 확보 및 관리 전략을 철저히 세워야 합니다. 또한, 초기 단계부터 제약사, 병원, 보험사 등 다양한 이해관계자들과의 긴밀한 소통을 통해 사업 모델의 실현 가능성을 검증하고, 잠재적 파트너십 기회를 모색하는 것이 성공적인 시장 안착에 필수적입니다. 개인의 상황에 따라 로드맵 실행 계획은 달라질 수 있으므로, 전문가와 상담하는 것을 권장합니다.
AI 신약 개발 로드맵의 상세 내용은 원본 글에서 확인하세요.