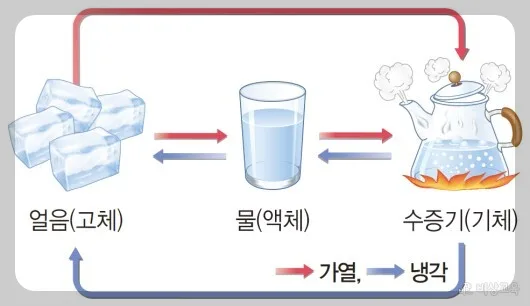
용매, 용질, 용액의 개념을 명확히 이해하는 것은 화학의 기초입니다. 2026년 현재, 이 용어들은 변함없이 물질의 혼합 상태를 설명하는 핵심 요소로 사용됩니다. 용매는 다른 물질을 녹이는 물질이며, 용질은 용매에 녹는 물질입니다. 이 둘이 합쳐져 균일하게 섞인 혼합물을 용액이라고 합니다.
용매, 용질, 용액의 정의와 차이점은 무엇인가요?
용매는 다른 물질을 녹여 용액을 만드는 역할을 합니다. 고체와 액체가 섞일 때는 액체가 용매가 되고, 두 액체가 섞일 때는 양이 더 많은 액체가 용매가 됩니다. 예를 들어, 물에 소금이 녹아 소금물을 만들 때 물이 용매입니다. 용질은 용매에 녹아 용액을 만드는 물질로, 고체, 액체, 기체 모두 용질이 될 수 있습니다. 탄산음료에서 이산화탄소가 용질에 해당합니다. 용액은 두 가지 이상의 물질이 균일하게 섞여 있는 혼합물로, 일반적으로 액체 용매에 고체, 액체, 기체 용질이 녹아 있는 상태를 말합니다. 우유나 과일 주스는 입자가 균일하게 퍼져 있지 않아 용액으로 분류되지 않는 경우가 많습니다.
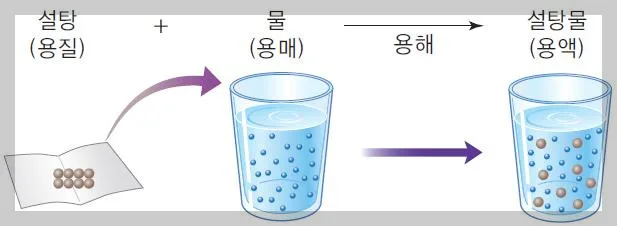
용해 현상이란 무엇이며, 용해도와 퍼센트 농도는 어떻게 계산하나요?
관련 글
용해는 용질이 용매에 고르게 섞여 용액이 되는 현상입니다. 이 과정이 일어나려면 용질과 용매 입자 사이의 인력이 중요합니다. 예를 들어 소금이 물에 녹는 것은 물 분자와 이온 사이의 인력이 소금 결정 내 이온들 사이의 인력보다 크기 때문입니다. 용해도는 특정 온도에서 용매 100g에 최대로 녹을 수 있는 용질의 양을 의미하며, 대부분 고체는 온도가 높을수록 용해도가 증가합니다. 퍼센트 농도는 용액 100g 속에 녹아 있는 용질의 g 수를 백분율(%)로 나타낸 것으로, 일상생활에서 용액의 진하기를 나타낼 때 가장 흔하게 사용됩니다. 예를 들어, 물 90g에 설탕 10g을 녹이면 총 용액 100g이 되므로, 설탕의 퍼센트 농도는 10%가 됩니다.
용액은 어떤 상태로 존재하며, 용매와 용질의 구분 기준은 무엇인가요?
용액은 액체 상태뿐만 아니라 고체 및 기체 상태로도 존재합니다. 합금은 고체 상태의 용액이며, 공기는 기체 상태의 용액입니다. 일반적으로 용질은 녹는 물질, 용매는 녹이는 물질로 구분하지만, 항상 명확하게 나뉘는 것은 아닙니다. 액체와 고체가 섞인 경우 액체를 용매, 고체를 용질로, 액체와 기체가 섞인 경우에도 액체를 용매, 기체를 용질로 봅니다. 두 액체나 두 기체가 섞인 경우에는 양이 많은 쪽을 용매, 적은 쪽을 용질로 구분합니다. 예를 들어, 에탄올과 물이 섞인 경우, 에탄올의 양이 더 많다면 에탄올이 용매가 됩니다.
용액과 용액이 아닌 혼합물을 구분하는 기준은 무엇인가요?
용액은 두 가지 이상의 물질이 완전히 균일하게 섞인 혼합물입니다. 따라서 용액의 어느 부분을 취해도 성질이 같고, 시간이 지나도 가라앉거나 떠오르는 물질이 없으며, 거름종이로 걸러지지 않습니다. 반면, 우유는 단백질이나 지방 입자가 물에 퍼져 있지만 균일하게 섞이지 않아 용액이 아닙니다. 과일 자체를 갈아 만든 주스는 시간이 지나면 층이 분리되거나 찌꺼기가 가라앉아 용액으로 보기 어렵습니다. 하지만 인공 향료로 만든 주스처럼 균일하게 섞여 있고 침전물이 생기지 않는다면 용액으로 간주될 수 있습니다. 이러한 균일성과 안정성은 용액과 비균일 혼합물을 구분하는 중요한 기준입니다.
자세한 내용은 원본 글에서 확인하세요.