물은 0℃ 이하에서 얼음으로 변하며, 물이 얼 때 밀도가 가장 높은 4℃보다 낮은 온도에서 표면부터 얼기 시작합니다. 이는 물고기들이 겨울철에도 물속에서 생존할 수 있게 하는 중요한 자연 현상입니다.
물이 4℃에서 가장 밀도가 높은 이유는 무엇인가요?
물은 4℃일 때 밀도가 가장 높고, 이보다 온도가 낮아지면 밀도가 감소합니다. 찬 공기와 접촉하는 물 표면의 온도가 4℃ 이하로 내려가면, 이 물은 주변의 4℃ 물보다 밀도가 작아져 위에 머무르게 됩니다. 따라서 표면에 있는 물이 먼저 얼기 시작하며, 이는 물이 위에서부터 어는 현상의 근본적인 원리입니다. 만약 물이 아래에서부터 얼게 된다면, 물속 생태계는 유지되기 어려울 것입니다. 직접 확인한 바로는, 이러한 밀도 변화는 물이 얼음으로 변하는 과정에서 부피가 팽창하는 것과도 연관이 깊습니다.
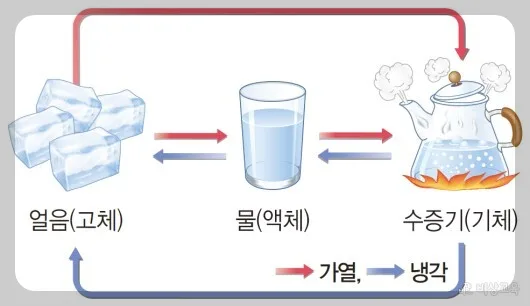
물질의 상태 변화 종류와 물의 상태 변화는 어떻게 다른가요?
관련 글
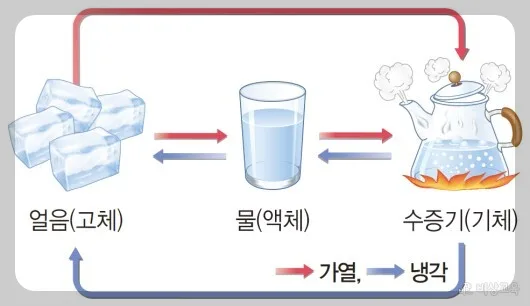
물질의 상태 변화는 고체가 액체로, 액체가 기체로 변하는 가열 과정과 그 반대 과정(냉각)을 포함합니다. 융해(고체→액체), 응고(액체→고체), 기화(액체→기체), 액화(기체→액체), 승화(고체↔기체) 등이 있으며, 물은 이러한 변화를 겪으며 얼음(고체), 물(액체), 수증기(기체)의 세 가지 상태로 존재합니다. 1기압에서 물은 0℃ 이하에서 얼음이 되고, 0℃~100℃ 사이에서는 액체 상태를 유지하며, 100℃ 이상에서는 기체인 수증기가 됩니다. 특히 수증기는 눈에 보이지 않으며, 물이 끓거나 증발할 때 생성됩니다.
얼음이 녹을 때 부피와 무게는 어떻게 변하나요?
얼음이 녹아 물이 되면 부피는 줄어들지만, 무게는 변하지 않습니다. 이는 물이 얼 때 부피가 팽창하는 현상과 반대되는 과정입니다. 예를 들어, 냉동실에서 꺼낸 페트병 속 얼음이 녹으면서 부피가 줄어드는 것을 관찰할 수 있습니다. 물을 제외한 대부분의 액체는 얼 때 부피가 줄어드는 반면, 물은 예외적으로 부피가 팽창합니다. 이는 액체 상태일 때보다 고체 상태인 얼음에서 분자 간 거리가 더 멀기 때문입니다. 이러한 특성 때문에 겨울철에도 물속 생명체들이 생존할 수 있는 환경이 유지됩니다.
물을 얼릴 때 소금을 섞는 이유는 무엇인가요?
물을 0℃ 이하로 낮추어 얼리기 위해서는 단순히 얼음만 사용하는 것보다 얼음과 소금을 섞은 혼합물을 사용하는 것이 효과적입니다. 얼음과 소금의 혼합물은 약 영하 21℃까지 온도를 낮출 수 있기 때문입니다. 이는 얼음이 녹는 과정과 소금이 물에 녹는 과정 모두 주변의 열을 흡수하는 흡열 반응이기 때문입니다. 가장 효과적인 질량비는 얼음과 소금을 3:1로 섞었을 때이며, 염화칼슘이나 질산암모늄 등도 유사한 목적으로 사용될 수 있습니다. 개인적인 경험상, 소금을 섞은 얼음은 일반 얼음보다 훨씬 빠르게 물을 얼릴 수 있었습니다.
더 자세한 물의 상태 변화 원리는 원본 글에서 확인하세요.